Mitglied bei
Eine weitere Suchmöglichkeit besteht darin, z.B. bei www.google.de das Suchwort einzugeben und dann nach einem Leerzeichen den Zusatz site:www.cfs-aktuell.de
Sie erhalten dann alle Seiten auf cfs-aktuell.de, auf denen der gesuchte Begriff vorkommt.
Artikel des Monats Januar 2011 Teil 7
Virale Genese des CFS - ist XMRV beteiligt?
Zusammenfassung des Vortrags von
Priv. Doz. Dr. Wilfried Bieger
anlässlich der Fatigatio-Fachtagung vom 24.-25. September 2010 in Dortmund
von Regina Clos
|
Bitte beachten Sie: 2012 hat sich herausgestellt, dass dieses XMRV keine Humaninfektion, sondern eine im Labor entstandene Chimäre war. Näheres unter Artikel des Monats Dezember 2012 - 1 auf dieser Website! |
Eine Postinfektiöse Fatigue ist nachgewiesen bei folgenden Infektionen: EBV, HHV6, CMV, ParvoB19, HBV, HCV, Enteroviren, Q-Fieber, Lyme-Borreliose. Reaktivierte Infektionen seien wahrscheinlich Sekundärphänomene des ursprünglichen Krankheitsgeschehens. Das gelte für EBV, HHV6, HHV7, CMV. Möglicherweise sei das CFS auch durch das Retrovirus XMRV bzw. HMRV verursacht. Man finde dabei immer eine Immundysfunktion im Sinne einer Immunaktivierung und Immundefizienz wie etwa einen NK-Zelldefekt und eine erhöhte CD8/T-Zellaktivität sowie zahlreiche proinflammatorische Zytokine, die auf eine Immunaktivierung bzw. ein infektiöses Geschehen hinweisen. Auch die Genexpression unterscheide sich von Gesunden auf charakteristische Weise. Er stellte zwei Fälle vor, in denen das Epstein-Barr-Virus und das Cytomegalie-Virus deutlich aktiv waren, und bis zu einem gewissen Grade würden die Patienten in solchen Fällen auch auf eine Behandlung ansprechen – man würde bei der Behandlung einzelner Phänomene durchaus einen Teilerfolg erzielen, aber den durchgreifenden Erfolg gäbe es erfahrungsgemäß dadurch nicht. Dr. Bieger diskutierte die Entdeckung des Retrovirus XMRV als möglichen diagnostischer Marker für CFS. Er hat in Zusammenarbeit mit einem der besten Retrovirologen und Molekularbiologen an der Uni Heidelberg gleich nach der Veröffentlichung der Science-Studie im Oktober 2009 versucht, das XMRV mit nPCR zu bestimmen, sie hatten aber zunächst keinen Erfolg. Möglicherweise hätte das daran gelegen, dass sie möglichst schnell nach der Probenentnahme die DNA aus dem Blut isoliert hätten, etwas, was nach Aussage von Dr. Mikovits dazu führe, dass man das Virus dann nicht mehr finde. Sie werden die Bestimmung des Retrovirus jetzt in enger Zusammenarbeit mit Mikovits erneut versuchen. (Anmerkung d. Red.: ein Ergebnis ist im Januar/Februar 2011 zu erwarten.) Die im August erschienene Arbeit von Lo/Alter, die das Retrovirus bei 86,6% der Patienten und bei 6,8% der Kontrollen gefunden haben, weise darauf hin, dass man mit dieser Entdeckung zumindest diagnostisch einen fundamentalen Schritt weiterkommen würde. Wenn es um die Diagnose des CFS geht und was man dabei messen kann, so finden wir oft reaktivierte Infektionen. Die Frage der Retroviren (XMRV/HMRV) ist noch nicht geklärt. Immundysfunktionen findet man oft, und was man immer findet, sind inflammatorische Prozesse, die sich über abweichende Zytokinwerte manifestieren (z.B. IL-1, IL-6, TNFa, IL-17,TH1, IL-2, IFNg, IL-12, TGFß, IL-10, IL-13,TH2, IL-4, IL-5, IL-8, IFN-g, NF-kB). Die Aktivierungsmuster dieser Zytokine sind bei MCS, CFS und Fibromyalgie jeweils unterschiedlich. Dr. Bieger kritisierte, dass CFS in Deutschland trotz all dieser messbaren und abweichenden Parameter vorwiegend als psychiatrische oder psychosomatische Erkrankung betrachtet wird weshalb auch keine Forschung stattfindet und alles aus USA kommt.Auch bei MCS finde man eine starke Zytokinaktivierung. Diese bilden ein Netzwerk, und wenn man die Beziehung zwischen den verschiedenen Zytokinen untersucht, wird deutlich, dass es bei CFS ein ganz anderes Muster gibt als bei Gesunden. Und auch dieses Muster rankt sich um das Thema Infektion. Was wir also wissen ist: das Immunsystem ist aktiviert, es besteht eine Dysfunktion und möglicherweise liegt eine reaktivierte, chronische Infektion vor. NF-kappa-b ist der empfindlichste Marker für eine Immunaktivierung, denn Nfkappa-b ist zentraler Schalter in allen Zellen. Daran kann man immer sehen, ob eine Immunaktivierung vorliegt, auch wenn man bei den anderen Werten nichts findet. Bei den folgenden Zytokinen finden sie bei allen Multisystemerkrankungen am häufigsten Abweichungen: (Folie 22 aus Dr. Biegers PPP-Vortrag)
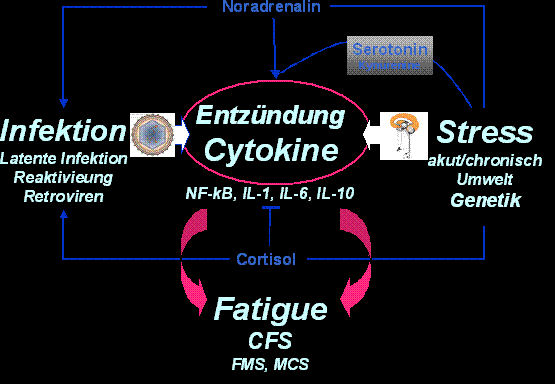
Es sei allerdings nicht zuverlässig, diese Werte im Blutplasma zu messen. Dort findet man sie nur bei einer relativ starken Aktivierung. In einer neueren Arbeit hat man die spezifischen Zytokinmuster von CFS-Patienten mit denen von Gesunden verglichen und charakteristische und deutliche Abweichungen gefunden, die am ehesten für eine infektiöse Genese sprechen. Was wir also bei allen offenen Fragen noch wissen ist, dass das Immunsystem aktiviert ist und eine Dysfunktion besteht, die möglicherweise die Ursache für die verstärkte Reaktivierung von latenten Infektionen ist. Und wir wissen, dass die Fatigue eine zentrale Folge dieser proentzündlichen Zytokine, speziell des IL1beta, im zentralen Nervensystem ist. Fatigue bzw. die sogenannten Sickness-Reaktionen sind eine zentrale Folge primär von Wirkungen proentzündlicher Zytokine. Bestimmte Personen reagieren auf Stressoren, also Infektionen, psychischen Stress, Medikamente etc., anders, nämlich mit einer inflammatorischen Reaktion, bei der Interleukine ausgeschüttet werden (TNFa, IL1ß, IL6, INFg, PgE2), und die wirken dann auf das zentrale Nervensystem, während die normale Stressreaktion von neuronellen Anpassungsreaktionen dominiert wird (CRH, AVP, Cortisol, Noradrenalin). Diese Sickness-Reaktion ist bei CFS chronifiziert. Sie kann durch verschiedene Stressoren zustande kommen, aber das zentrale Problem bei CFS sind nach seiner Überzeugung Infektionen. Alle Stressoren wirken in unterschiedlich starkem Ausmaß auf vier Systeme: das Immunsystem, das zentrale und das autonome Nervensystem und die Hypothalamus-Hypophysen-Nebennieren-Achse. Zwischen all diesen Systemen gibt es komplexe Wechselwirkungen, d.h. jeder zentrale Stressor wirkt auch auf die Peripherie, und jeder periphere Stressor wirkt auch zentral. Eine Infektion wirkt also immer auch auf das zentrale Nervensystem. Das NF-kappa B ist der zentrale Schalter, der zu einem sich selbst verstärkendem Kreislauf führt. Es gibt vielfältige und komplexe Wechselwirkung zwischen immunologischen, neurologischen Steuerungsmechanismen, die sowohl durch Infektionen als auch durch andere Stressoren beeinflusst werden. Auch genetische Faktoren spielen eine Rolle. Dr. Bieger diskutierte an einem Fallbeispiel mit völliger Dysregulation der HPA-Achse die mögliche Rolle des Cortisols. Sie finden oft Fälle, bei denen das Cortisol niedrig ist, bzw. nicht mehr genügend ausgeschüttet wird, d.h. die Stressadaption findet nicht mehr adäquat statt. Es gibt eine Blockade der Hypophysen-Hypothalamus-Nebennieren-Achse, aber die kommt nicht von der Nebenniere, sondern liegt auf der Ebene des Hypothalamus durch eine Rezeptor-Downregulation. An einem weiteren Fallbeispiel mit einem Serotonindefizit diskutierte er die Frage, worauf das oft feststellbare extreme Defizit an Neurotransmittern (Adrenalin, Noradrenalin Dopamin, Serotonin) liegen könne. Sie reagieren sehr empfindlich auf Stressoren. Es gibt eine komplexe Wechselwirkung zwischen inflammatorischer Situation und Neurotransmittern. Eine chronische Aktivierung auf entzündlicher Ebene führt zu einem Serotoninmangel. Antidepressiva, die zu einer Erhöhung des Serotoninspiegels führen, wirken wahrscheinlich genau aus diesem Grund – nicht, weil bei den Patienten eine Depression im Vordergrund steht, sondern weil sie antiinflammatorisch wirken. Auch Genexpressionsstudien und Genpolymorphismusstudien stützen das – man findet Genvariationen in den Bereichen der Gene, die an der Hypophyse-Hypothalamus-Nebennieren-Achse beteiligt sind. Die meisten CFS-Patienten haben ein oder mehrere dieser genetischen Varianten, die die Funktion von Noradrenalin, Serotonin, Cortisol + GC-Rezeptor, CRH + CRH-Rezeptor und Inflammation betreffen. Es ist also auf der einen Seite die Stressbewältigung und auf der anderen die Inflammation betroffen. Was ist also der aktuelle Stand bei CFS? Wir haben Inflammation, wir haben Stress, wir haben die Cytokine, und alle wirken in Richtung Fatigue. Mit diesem zentralen Gebiet hätten wir uns zu beschäftigen. Er würde sich jedoch sehr freuen, wenn das Retrovirus XMRV/HMRV uns den Schlüssel zu der Frage liefern würden, was CFS ist. (Folie 39 aus Dr. Biegers PPP-Vortrag)
|